白血病病毒的“隐形面纱”被掀开:HTLV‑1沉默元件揭示潜伏真相
隐藏了半个世纪的“开关”终于亮起
2025年5月13日,资深医疗专家关注到熊本大学人类逆转录病毒联合研究中心Satou教授团队在国际期刊《Nature Microbiology》发布的重要成果:他们首次鉴定出人类T细胞白血病病毒1型(HTLV‑1)基因内部的一段“沉默元件”(viral silencer),揭示了病毒如何长期在人体中“隐身”,并指出了未来逆转录病毒治疗的新方向。
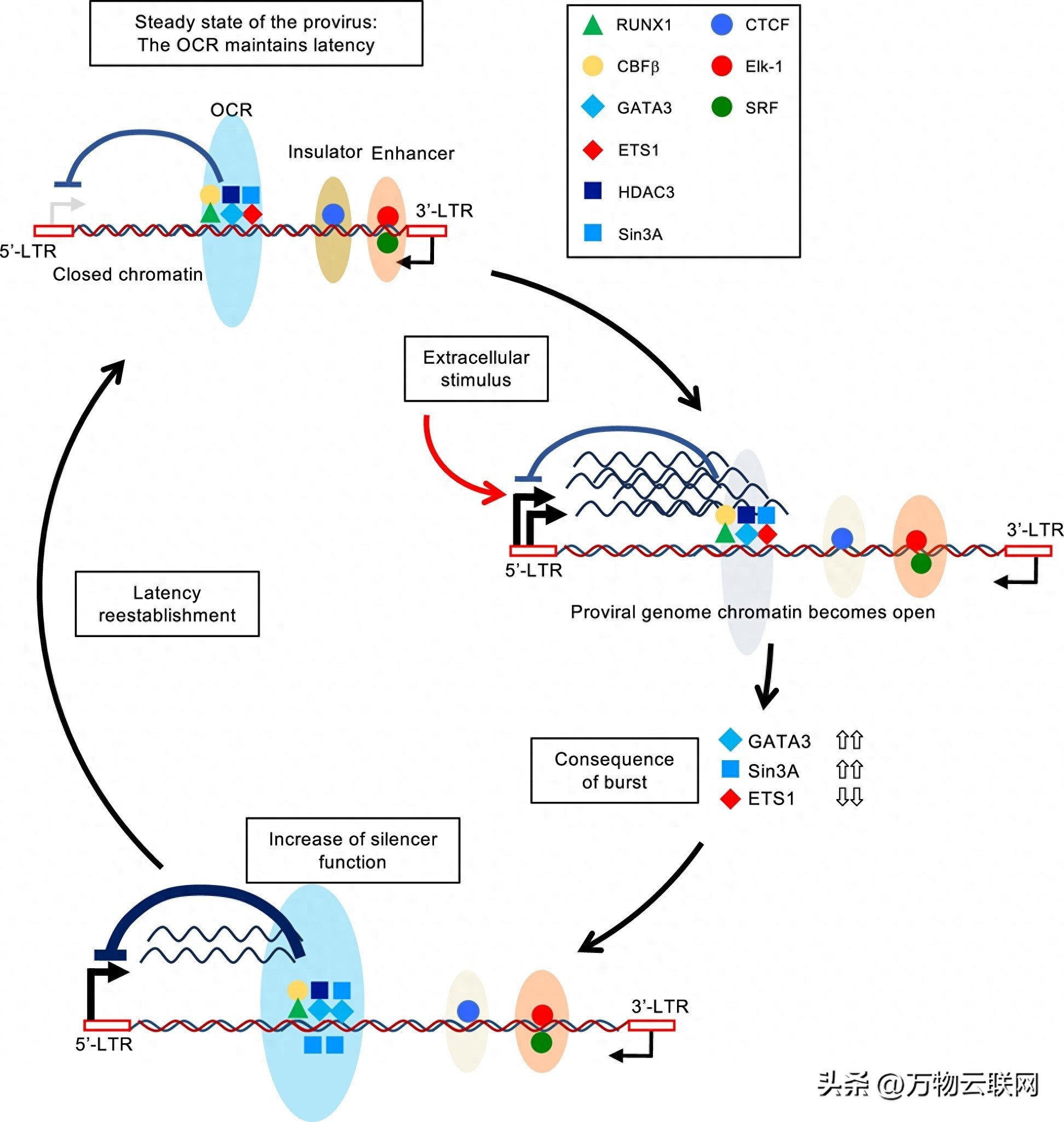
HTLV-1潜伏期分子机制示意图。图片来源:《自然》(侵删)
HTLV‑1:为何长期潜伏,却危险潜藏
- 什么是HTLV‑1?
HTLV‑1是一种极可能导致成人T细胞白血病/淋巴瘤(ATL)的致癌型逆转录病毒。全球约有2,000万人感染,其中日本约100万人携带,该国尤其在九州与冲绳地区是高发区。大多数携带者终身无明显症状,但约**2%~5%**会在数十年后快速进展为ATL或炎症性病变。 - 为何不被免疫系统识别?
病毒整合进入宿主的T细胞染色体后,进入“潜伏”(latent)状态,极少表达病毒蛋白,因此不会激活免疫反应,从而取得长期共存。
重大突破:沉默元件如何运转病毒“隐身术”
- 隐藏在病毒基因里的“静默开关”
Satou团队通过最新的ATAC‑seq与ChIP‑seq技术,锁定HTLV‑1在感染者外周CD4⁺T细胞中的一个“开放染色质区域(OCR)”。这一区域事实上能绑定位宿主的转录因子RUNX1(以及GATA3/ETS1等辅助因子),使病毒5′ LTR启动子“关灯”式沉默,进入极低表达状态。 - 脱除沉默元件,立即“曝光”
携带该区域突变的HTLV‑1在实验细胞中病毒产量显著增加,更容易被细胞毒性T细胞识别并清除,说明沉默元件是潜伏关键 。
更惊人的是:把它“嫁接”给HIV
研究者将HTLV‑1的沉默元件插入HIV‑1基因组中,结果该改造病毒“变得更沉默”:复制力下降,细胞杀伤效应明显减弱,呈现出类似HTLV‑1的潜伏作用 。
"This is the first time we've uncovered a built‑in mechanism that allows a human leukemia virus to regulate its own invisibility,"
—— Satou教授如是说。
“这是一种进化上的巧妙策略;如今我们已理解它,就有机会‘反其道而行’。”
实用启示:三个维度展现未来医学价值
应用方向 | 含义与前景 |
治疗HTLV‑1/ATL | 可研发小分子或RNA药物,专门“拆除”沉默元件或阻断RUNX1结合,让潜伏病毒一举被免疫系统识别清除;也可以开发植入式沉默元件载体,实现病毒精准“唤醒”或“压制”。 |
辅助HIV长期控制 | 若将沉默元件整合到HIV载体中,可研究是否能实现低复制、低炎症的“深潜型”感染者状态,从而大幅降低抗逆转录病毒治疗(ART)的毒副作用及耐药风险。 |
基因编辑+细胞疗法创新 | 借助CRISPR/Cas9技术,可将沉默元件精准植入特定病毒位点,形成可控的「病毒沉默/激活开关」系统,作为下一代抗病毒平台。 |
产业洞察:潜在市场规模之大不可轻视
- HTLV‑1相关ATL治疗市场
2024年全球ATL治疗隐性市场估计在12亿–18亿美元之间,预计到2033年有望翻倍至25亿美元以上,年均增长率约为9%。 - HIV抗病毒药物市场
2022年全球HIV疗法市场规模约103亿美元,预计到2030年将攀升至113亿美元(复合年均1.5%增长)甚至更快扩张至超300亿美元(若考虑宽定义周边策略)。 - 临床试验与基因疗法资金盛宴
全球HIV临床试验市场2024年约为15.6亿美元,预计到2030年突破21亿美元。如此创新靶点如沉默元件,一旦推动基因治疗或细胞疗法落地,预示巨量资本与专利前景。
资深医疗专家小结:
“HTLV‑1用了数万年进化出的‘隐藏开关’,现在人类科学正巧切入这一机制核心;了解它,就能将病毒自带的武器‘反向控制’,发明出精准、安全的新疗法。这不仅将改变ATL的治疗方式,也可能为HIV感染者带来革命性控制策略。”
如今,这一技术正处于早期科研阶段,但所打开的路径,已不再是纸上谈兵,而可能成为未来基因药或细胞疗法的新方向。不管是药企、投资机构,还是科研机构,都应高度关注这一领域的下一个风口。
